图片来源:Jeff Fitlow / Rice University

图片来源:Jorge Vidal
黄声希与王子洋谈阿尔茨海默病分子图谱:不染色,不标记,也不预设寻找目标
在过往大部分历史中,阿尔茨海默病研究都处于一种必然的收缩状态。面对极其复杂的疾病,科学家选定目标,如淀粉样蛋白斑块与 tau 蛋白缠结,并围绕其建立方法。所用工具虽然强大精准,却属于特定维度的精准:研究者选定分子,设计标记物,随后看见预设的目标。
SCOPE 实验室遵循不同逻辑。该方法不以目标为起点,而以问题开始:组织中究竟存在什么,分布在何处?其利用拉曼光谱技术,通过物质散射光的方式读取分子指纹,从而观察大脑组织的天然化学状态。无染料,无荧光标记,不对存在物做任何预先承诺。 这一结果构成了首个无标记生成的阿尔茨海默病全脑分子图谱。该图谱由数千个重叠的光谱测量点逐层构建,并经由机器学习算法分析,能够识别出人类感官无法察觉的模式。最终揭示出一种并不局限于斑块且分布并不均匀的疾病。与之相关的化学变化以不规则、区域特异性的模式分布于全脑。在与记忆最相关的区域,海马体和皮质,胆固醇与糖原代谢的紊乱与预料中的淀粉样蛋白积累一同显现。 黄声希从光学光谱与纳米材料领域跨界而来,而非出自生物学背景。在她看来,大脑与她职业生涯中研究的薄层材料具有某种共同点:它位于基底,具有分层结构,并蕴含着光可读取的分子信息。王子洋主导了技术开发,最初他仅测量大脑的一小块区域,随后提出了一个简单的问题:如果我们绘制整个大脑会怎样?最终出现的并非对已知事物的印证,而是一张挑战传统视角的地图。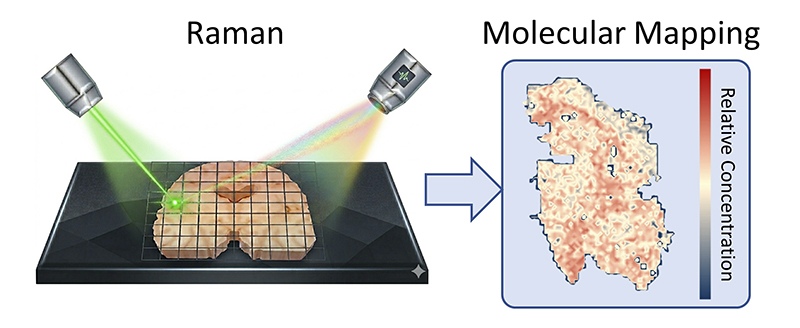
图片来源:Ziyang Wang / Shengxi Huang Research Group, Rice University
对话
黄声希:我早期受训于光学光谱与纳米材料领域。我曾研究二维材料与有机分子的相互作用,发现某些二维材料能增强特定分子的拉曼信号。于是我开始思考这种效应是否适用于更复杂的生物分子,并转化为实际应用。博士阶段后期,我开始接触生物分子,结果令人振奋。建立研究组后,我决定利用这种独特现象深耕生物传感领域。作为教职人员拥有追求独特想法的自由。幸运的是,我遇到了优秀的合作者,他们教授我大量阿尔茨海默病知识并提供样本,促成了目前的成果。
黄声希:对我们而言,大脑切片就像一块二维材料:它是平坦的,位于基底之上,并携带我们可以测量的拉曼信号。大脑更令人兴奋之处在于其多功能性,这里有海量的分子信息等待解密。通过相对简单的二维材料拉曼信号,我们已能表征缺陷、应变、厚度和氧化情况。面对大脑更丰富的信号,我们能学到的东西远不止于此。由于数据复杂度极高,有时需要 AI 辅助理解特定特征,而这正是电气工程师的强项。这种看似迥异的领域间存在如此多共同点,令人欣慰。
王子洋:捕捉大脑“原貌”意味着在不引入可能产生观察偏差的标记物情况下,观察其天然分子状态。传统染料与荧光标记要求预先决定突出显示哪种分子,往往导致研究聚焦于已知目标,忽略了组织更广泛的化学环境。无标记方法允许我们直接测量大脑内在的分子指纹。我们不再仅仅寻找预设标记物,而是观察完整的分子景观,探测那些可能被隐藏的细微生化变化,从而全方位理解疾病。
王子洋:过往研究多聚焦于特定区域或已知病理标志。我们希望拓宽视野,询问疾病相关的分子变化如何在全脑分布。超光谱拉曼成像与 AI 技术的进步使扫描大尺寸脑截面成为可能。最令我们惊讶的是,病理相关的分子变化并不局限于单一区域。图谱揭示出空间模式与区域演进,表明阿尔茨海默病涉及比此前认知更广泛的生化改变。
王子洋:我们的发现表明,该病涉及更广泛的代谢紊乱,而不止是错误折叠蛋白的积累。虽然斑块与缠结仍是重要标志,但全脑范围内胆固醇和糖原的变化更为显著。这表明该病可能涉及系统性代谢失衡,影响脑细胞能量使用和脂质调节。我们的结果提示,不应仅将其视为局部的蛋白质聚集,它反映了脑细胞维持代谢方式更深层的生化改变。
黄声希:在生物医学中,许多如 MRI、mass spectrometry、X-ray imaging、CT 等工具最初由物理学家开发,随后在医学领域大放异彩。拉曼光谱的故事亦是如此。这些工具能为理解疾病提供新鲜视角。跨学科工作的迷人之处在于,外部视角有时能带来领域内专家难以触及的发现。
王子洋:机器学习协助我们在极端复杂的数据中探测模式,但它无法取代科学推理。算法能突出人类难以直接识别的细微分子特征。然而,科学家在提出正确问题、设计实验以及从生物学角度解读模式含义方面,依然不可替代。人类直觉引导假设,并确保结果符合病理逻辑。机器学习是发现的利器,而人类洞察力仍是理解与验证的核心。
黄声希:的确,利用光线读取大脑分子状态具有特殊意义。拉曼光谱通过光与分子的相互作用揭示隐藏的生化变化。虽然大部分工作属于收集光谱、分析数据等技术劳动,但偶尔退后一步思考这些工具揭示的内容,确实令人心生感触。它提醒我们,所有技术工作的目标都是为了更深入地理解疾病,并助力早期检测与治疗。
黄声希:我们实验室整体关注传感技术。大脑项目涉及传感与疾病相关的分子,而二维及量子材料研究也服务于此目标。通过选择合适的二维材料接触生物样本,测量信号可获得显著增强。我们通过对二维材料进行原子级工程改造以产生新特性。这种基础研究可能开启全新的量子传感机制,提供传统技术无法企及的精度。
王子洋:研究者可能从关注单一生物标志物转向调查分子变化如何在全脑扩散。科学家不再仅询问特定蛋白是否存在,而是考察脂质代谢等生化通路随空间演变的过程。我希望这种方法能解答此前难以触及的问题:识别病理显现前的早期分子变化,理解不同脑区间的相互影响,并发现神经退行性变中全新的生化通路。
结语
黄声希所描述的科研态度中蕴含一种特殊的谦逊:坚信新鲜视角有时能看见长期熟悉者无法发现的事实。她的实验室并非带着待证实的理论进入该领域,而是带着一种技术,以及探究未知的耐心。
这一发现既是结果,也是挑战。阿尔茨海默病并非蛰伏于一处,也不仅是蛋白聚集的故事。它是分布于整个器官、极不均匀的化学破坏,存在于胆固醇与糖原代谢中,存在于记忆曾驻留的生化环境里。王子洋在项目开始时曾问:如果我们能看见大脑全貌会怎样?答案比单一蛋白的故事更奇特,也更复杂。这种被精准测量的奇特性,正是新事物的开端。


黄声希与王子洋谈阿尔茨海默病分子图谱
自开始关注阿尔茨海默病领域以来,一个问题始终困扰着我:为何在经历数十年的研究、针对单一分子目标投入数十亿美元后,该病依然难以治愈?当我读到莱斯大学黄声希教授 SCOPE 实验室的工作时,感到一种全新的观察方式正在降临。该团队来自生物学领域之外,利用光线读取处于原始化学状态的大脑组织。
这项发表在 2026 年初《ACS Applied Materials and Interfaces》上的研究,首次制作出动物模型中阿尔茨海默病大脑的完整无标记分子图谱。通过超光谱拉曼成像与机器学习,团队逐层绘制了整个大脑的化学变化,过程中未引入任何染料或分子标记。最终发现的事实远超淀粉样蛋白斑块的范畴。
黄教授与该研究第一作者、莱斯大学电气与计算机工程博士生王子洋共同撰写了下文回复。他们在发布前对技术准确性进行了校审。
——Adelina在过往大部分历史中,阿尔茨海默病研究都处于一种必然的收缩状态。面对极其复杂的疾病,科学家选定目标,如淀粉样蛋白斑块与 tau 蛋白缠结,并围绕其建立方法。所用工具虽然强大精准,却属于特定维度的精准:研究者选定分子,设计标记物,随后看见预设的目标。
SCOPE 实验室遵循不同逻辑。该方法不以目标为起点,而以问题开始:组织中究竟存在什么,分布在何处?其利用拉曼光谱技术,通过物质散射光的方式读取分子指纹,从而观察大脑组织的天然化学状态。无染料,无荧光标记,不对存在物做任何预先承诺。
这一结果构成了首个无标记生成的阿尔茨海默病全脑分子图谱。该图谱由数千个重叠的光谱测量点逐层构建,并经由机器学习算法分析,能够识别出人类感官无法察觉的模式。最终揭示出一种并不局限于斑块且分布并不均匀的疾病。与之相关的化学变化以不规则、区域特异性的模式分布于全脑。在与记忆最相关的区域,海马体和皮质,胆固醇与糖原代谢的紊乱与预料中的淀粉样蛋白积累一同显现。
黄声希从光学光谱与纳米材料领域跨界而来,而非出自生物学背景。在她看来,大脑与她职业生涯中研究的薄层材料具有某种共同点:它位于基底,具有分层结构,并蕴含着光可读取的分子信息。王子洋主导了技术开发,最初他仅测量大脑的一小块区域,随后提出了一个简单的问题:如果我们绘制整个大脑会怎样?最终出现的并非对已知事物的印证,而是一张挑战传统视角的地图。

图片来源:Ziyang Wang / Shengxi Huang Research Group, Rice University
黄声希:我早期受训于光学光谱与纳米材料领域。我曾研究二维材料与有机分子的相互作用,发现某些二维材料能增强特定分子的拉曼信号。于是我开始思考这种效应是否适用于更复杂的生物分子,并转化为实际应用。博士阶段后期,我开始接触生物分子,结果令人振奋。建立研究组后,我决定利用这种独特现象深耕生物传感领域。作为教职人员拥有追求独特想法的自由。幸运的是,我遇到了优秀的合作者,他们教授我大量阿尔茨海默病知识并提供样本,促成了目前的成果。
黄声希:对我们而言,大脑切片就像一块二维材料:它是平坦的,位于基底之上,并携带我们可以测量的拉曼信号。大脑更令人兴奋之处在于其多功能性,这里有海量的分子信息等待解密。通过相对简单的二维材料拉曼信号,我们已能表征缺陷、应变、厚度和氧化情况。面对大脑更丰富的信号,我们能学到的东西远不止于此。由于数据复杂度极高,有时需要 AI 辅助理解特定特征,而这正是电气工程师的强项。这种看似迥异的领域间存在如此多共同点,令人欣慰。
王子洋:捕捉大脑“原貌”意味着在不引入可能产生观察偏差的标记物情况下,观察其天然分子状态。传统染料与荧光标记要求预先决定突出显示哪种分子,往往导致研究聚焦于已知目标,忽略了组织更广泛的化学环境。无标记方法允许我们直接测量大脑内在的分子指纹。我们不再仅仅寻找预设标记物,而是观察完整的分子景观,探测那些可能被隐藏的细微生化变化,从而全方位理解疾病。
王子洋:过往研究多聚焦于特定区域或已知病理标志。我们希望拓宽视野,询问疾病相关的分子变化如何在全脑分布。超光谱拉曼成像与 AI 技术的进步使扫描大尺寸脑截面成为可能。最令我们惊讶的是,病理相关的分子变化并不局限于单一区域。图谱揭示出空间模式与区域演进,表明阿尔茨海默病涉及比此前认知更广泛的生化改变。
王子洋:我们的发现表明,该病涉及更广泛的代谢紊乱,而不止是错误折叠蛋白的积累。虽然斑块与缠结仍是重要标志,但全脑范围内胆固醇和糖原的变化更为显著。这表明该病可能涉及系统性代谢失衡,影响脑细胞能量使用和脂质调节。我们的结果提示,不应仅将其视为局部的蛋白质聚集,它反映了脑细胞维持代谢方式更深层的生化改变。
黄声希:在生物医学中,许多如 MRI、mass spectrometry、X-ray imaging、CT 等工具最初由物理学家开发,随后在医学领域大放异彩。拉曼光谱的故事亦是如此。这些工具能为理解疾病提供新鲜视角。跨学科工作的迷人之处在于,外部视角有时能带来领域内专家难以触及的发现。
王子洋:机器学习协助我们在极端复杂的数据中探测模式,但它无法取代科学推理。算法能突出人类难以直接识别的细微分子特征。然而,科学家在提出正确问题、设计实验以及从生物学角度解读模式含义方面,依然不可替代。人类直觉引导假设,并确保结果符合病理逻辑。机器学习是发现的利器,而人类洞察力仍是理解与验证的核心。
黄声希:的确,利用光线读取大脑分子状态具有特殊意义。拉曼光谱通过光与分子的相互作用揭示隐藏的生化变化。虽然大部分工作属于收集光谱、分析数据等技术劳动,但偶尔退后一步思考这些工具揭示的内容,确实令人心生感触。它提醒我们,所有技术工作的目标都是为了更深入地理解疾病,并助力早期检测与治疗。
黄声希:我们实验室整体关注传感技术。大脑项目涉及传感与疾病相关的分子,而二维及量子材料研究也服务于此目标。通过选择合适的二维材料接触生物样本,测量信号可获得显著增强。我们通过对二维材料进行原子级工程改造以产生新特性。这种基础研究可能开启全新的量子传感机制,提供传统技术无法企及的精度。
王子洋:研究者可能从关注单一生物标志物转向调查分子变化如何在全脑扩散。科学家不再仅询问特定蛋白是否存在,而是考察脂质代谢等生化通路随空间演变的过程。我希望这种方法能解答此前难以触及的问题:识别病理显现前的早期分子变化,理解不同脑区间的相互影响,并发现神经退行性变中全新的生化通路。
黄声希所描述的科研态度中蕴含一种特殊的谦逊:坚信新鲜视角有时能看见长期熟悉者无法发现的事实。她的实验室并非带着待证实的理论进入该领域,而是带着一种技术,以及探究未知的耐心。
这一发现既是结果,也是挑战。阿尔茨海默病并非蛰伏于一处,也不仅是蛋白聚集的故事。它是分布于整个器官、极不均匀的化学破坏,存在于胆固醇与糖原代谢中,存在于记忆曾驻留的生化环境里。王子洋在项目开始时曾问:如果我们能看见大脑全貌会怎样?答案比单一蛋白的故事更奇特,也更复杂。这种被精准测量的奇特性,正是新事物的开端。