运动肌肉释放的蛋白质,如何成为保护老化大脑的关键,且无需触碰淀粉样蛋白斑块
对话
第一部分:斑块与持久性的悖论
Henriette van Praag 斑块与认知功能下降之间的联系,并不像大众想象中那样牢固。尸检研究表明,部分个体大脑中虽有斑块,却依然保持着完整的认知功能。因此,就实际功能而言,拥有斑块并不等同于患上痴呆症。虽然在实验小鼠模型中,斑块的数量或密度没有直接减少,但研究团队尚未观察斑块本身的成分,例如其密集程度或毒性水平如何。
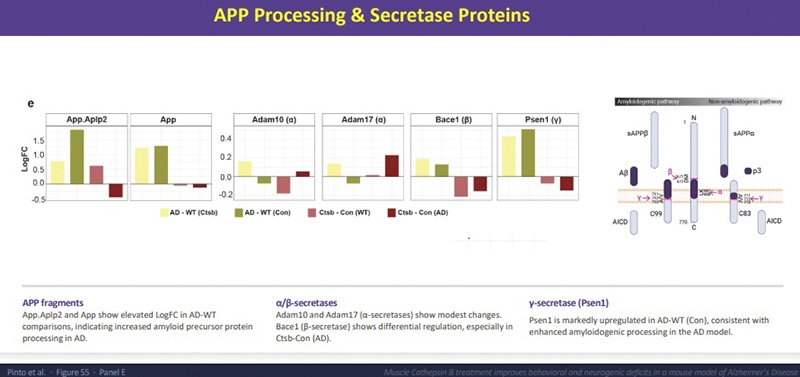
我可以说明的是,在蛋白质组学分析中,我们确实看到淀粉样蛋白在分子水平上的处理过程发生了变化。淀粉样前体蛋白(APP)以及产生毒性片段的酶(如 BACE1)有所减少;与此同时,参与非淀粉样生成途径的酶 ADAM10 和 ADAM17 则有所增加。我们还发现,Psen1(一种参与产生最具毒性淀粉样片段的 γ-分泌酶 )在未经治疗的阿兹海默症小鼠中显著上调,而治疗手段修正了这一模式。所以这并非一个简单的「是」或「否」的问题,而是在组织学上斑块看似未变的情况下,淀粉样蛋白的环境其实已经得到了优化。
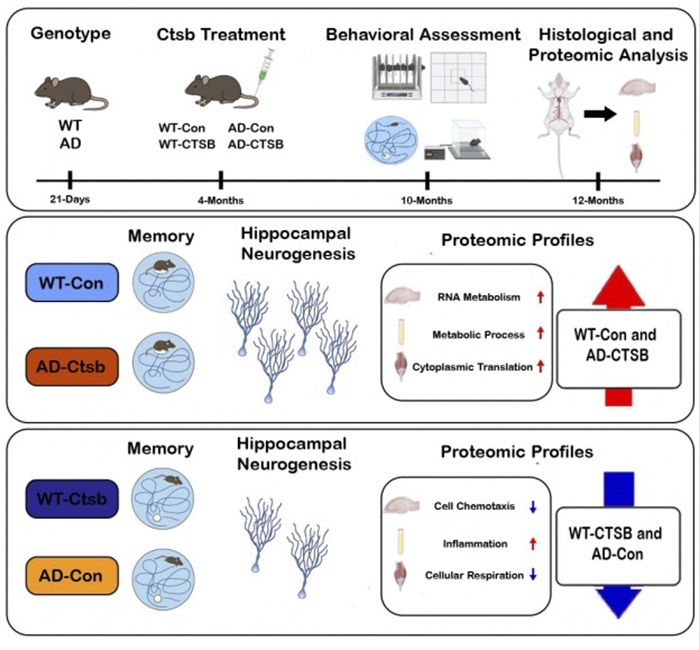
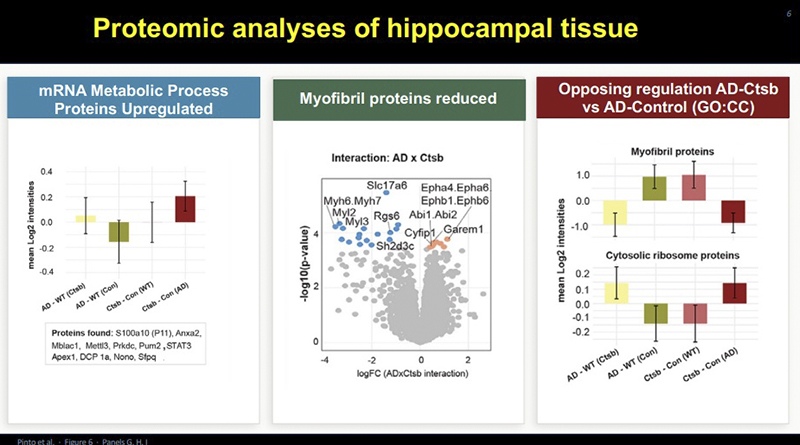
Henriette van Praag 这其中可能涉及多个机制。首先,mRNA 代谢过程相关的蛋白质水平有所上调,进而引起了与成年神经发生及突触可塑性相关蛋白质水平的变化,其中包括调节神经兴奋与抑制平衡的蛋白质。在阿兹海默症中,通常存在一种过度兴奋性,这会导致所谓的兴奋性毒性。Cathepsin B 治疗降低了谷氨酸蛋白水平,并增强了 GABA 能途径,这表明神经网络正在从内部重新建立平衡。
另一个观察结果是,在阿兹海默症小鼠的大脑中,我们发现肌原纤维蛋白有所增加。这类蛋白质主要在肌肉中表达,此前已有研究报道其在人类大脑老化和神经退行性病变中会增多。我们的治疗减少了这类蛋白质的存在,使大脑恢复到健康的受控水平。
第二部分:分子机制与进化背景
Henriette van Praag 我没有一个确切的进化答案,但我们观察到的模式是惊人的。肌肉中发生的情况与大脑中发生的情况高度一致。在大脑中,我们看到 RNA 代谢增加;在肌肉中,我们看到细胞质翻译和代谢过程得到改善。大脑并非在独自行动,而肌肉也不是在做完全无关的事情。它们似乎在协同工作,作为一个相互连接的系统。
Henriette van Praag 这属于本质上的差异。疾病状态显然改变了大脑对治疗的反应,同时也可能影响了肌肉对该蛋白质的代谢机制。至于这些变化具体如何影响下游的连锁反应,仍需进一步研究来厘清。
第三部分:治疗转化
Henriette van Praag 通过基因疗法使骨骼肌表达 Cathepsin B 确实具有可行性。若能进一步研究认知障碍患者与健康人群的肌肉组织,并观察其细胞在实验室环境中对载体的反应,将具有极高的学术价值。这不仅有助于医疗专业人员筛选患者,更能精确判断该项干预措施的适用性。对于那些肌肉已产生病变且无法维持规律运动的群体,未来或许可以通过这种方式识别并接受治疗。然而,距离开发出安全且适用于人体的干预手段仍有许多挑战待克服,后续必须进行更深入的临床前研究。
Henriette van Praag 这正是我所思考的,也是我们上面讨论的内容。活检或血液检测可能是监测早期变化的一种方式。风险是否可以提前 20 年被识别目前仍是未知数,但在认知症状出现之前,通过肌肉健康状况来预测风险,非常符合这项研究指向的方向。
第四部分:挑战与局限
Henriette van Praag Sarcopenia 肌肉减少症(即随老化而产生的肌肉质量临床性下降)在统计学上与认知功能衰退有显著关联。维持肌肉健康不仅是为了增强力量,对大脑健康同样至关重要。我们通常建议老年人进行力量训练,这不仅能维持肌肉量,更能活化代谢功能,并可能优化肌肉向全身释放的信号特征。
Henriette van Praag 关键在于浓度水平。在某些癌症案例中,血液中 Cathepsin B 的浓度远高于运动所产生的水平,这类高浓度往往与较差的预后相关。在运动产生的生理范围内,其背景、组织来源和浓度是完全不同的。
第五部分:阿兹海默症照护的未来
Henriette van Praag 我非常同意我们不应该孤立地治疗大脑。一个全面的方法,包含身体活动、健康的饮食以及提高整体的代谢健康,将大有助于延缓甚至预防疾病的发作。这也是我接受采访的原因,希望你能将这个建议传达给每一个人,毕竟我只是名科研工作者。
Henriette van Praag 哦,是的,可能有數百個。肌肉是一個巨大的內分泌器官,可能性非常高,或许还有数百种。肌肉具备强大的内分泌功能,Cathepsin B 的介入极可能影响肌肉分泌物的整体组成。要全面鉴定这些肌动蛋白,尤其是精确掌握它们与大脑间的信号对话机制,目前的探究仅仅是冰山一角。
结论
Henriette van Praag 的研究表明,大脑并非孤立地衰老。它与驱动其运动的肌肉保持着不间断的对话。当这种对话中断,即久坐不动的生活方式导致肌肉分子信使流失,或肌肉减少症削减了维持神经可塑性的循环肌动蛋白时,大脑便失去了一个至关重要的韧性来源,且可能无法仅凭自身力量恢复。
Cathepsin B 虽未能清除斑块,但它似乎在一定程度上挽救或修复了被斑块破坏的功能:大脑产生新神经元的能力、平衡自身兴奋与抑制的能力,以及维持健康心智蛋白质图谱的能力。这绝非小事。推动阿兹海默症研究下一章节的关键问题,或许不再是如何移除已经堆积的物质,而是如何恢复已经失去的功能。
事实证明,答案可能并非始于神经内科病房,而是始于健身房。