
高建群博士的尼康微观世界2022年显微摄影大赛获奖作品有助了解神经退行性疾病
翻译: 高建群博士
尼康微观世界2022年显微摄影大赛刚刚公布了今年的获奖者。我们很高兴能邀请高建群博士讨论他的神经干细胞(NSCs)衍生的人类神经元的获奖作品和他的研究方向。作为前上海顶级神经内科医师,现任澳大利亚悉尼大学中央临床学院脑与心智中心,Glenda Halliday教授实验室研究的神经学家/神经科学家,高博士一直致力于理解和寻找解决帕金森、阿尔茨海默病等神经退行性疾病的诊治难点。
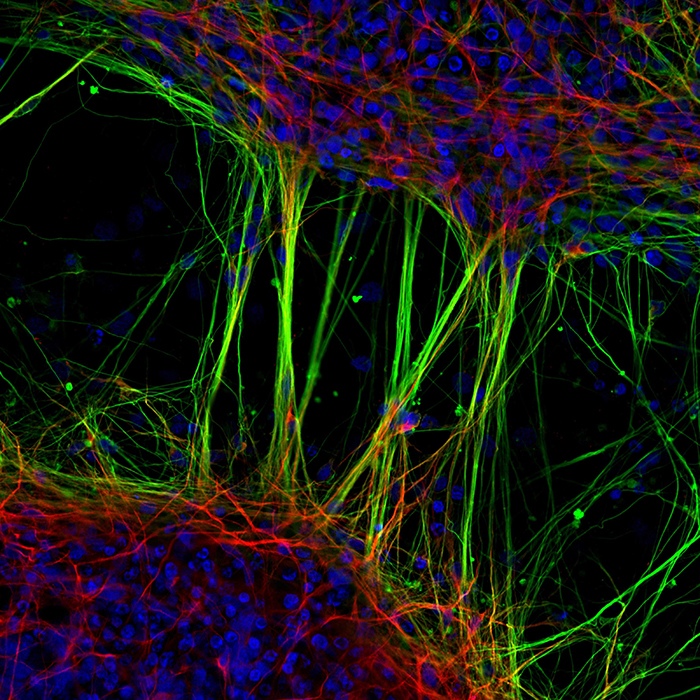
这张获奖作品是在培养多能干细胞、染色和图像拍摄方面进行的许多艰苦试验的结果。最终,高博士使用先进的尼康C2共聚焦显微镜捕捉到了这张清晰的图像。它帮助高博士和他的研究团队进一步了解导致帕金森病的机制,并引领未来开发神经退行性疾病的新治疗策略。
问:恭喜您拍摄的源⾃神经⼲细胞(NSC)的⼈类神经元的图像赢得了久负盛名的尼康微观世界2022年显微摄影⼤赛的前10名。请告诉我们您成为杰出显微摄影师的背景和培训。
答:作为⼀名在上海三级甲等医院临床⼯作多年的神经内科医⽣,我在见证医疗发展的同时也发现了很多悬⽽未决的医学问题值得去探索。我想在脑科学领域进⾏更深的探索。因此,我在澳⼤利亚悉尼⼤学临床医学院的脑研究中⼼(the Brain & Mind Center, Central Clinical School of the University of Sydney)完成了我的博⼠研究。悉尼⼤学的这所脑研究中⼼是⼀所世界尖端的研究机构,在那⾥,我专门研究⼈类脑神经元,以揭开其在帕⾦森、阿尔兹海默症等神经退⾏性疾病中的奥秘。很荣幸能加⼊到Halliday教授的团队,她是澳⼤利亚和世界顶尖的神经病理学专家,在Halliday实验室,我学到了许多神经科学领域研究的技术,也从事着令⼈兴奋的研究,我们在帕⾦森细胞模型中⾸度报道了TLR2在⼈神经元内发挥其免疫机理,在复杂的信号转导通路上找到物质作⽤的靶点,并⽤⼩分⼦抑制剂抑制帕⾦森病引起的异常蛋⽩积聚。⽆数个令⼈兴奋的时刻是我在科学道路上前进的动⼒。 这次是我因神经⼲细胞的共聚焦显微镜图⽚⽽第四次在Nikon Small World的⽐赛中获奖,感谢导师Glenda Halliday教授和同事们⼀直以来对我的⽀持和⿎励。因为这⽅⾯的研究,我曾获得过2018年度澳⼤利亚卫⽣部(NHMRC)为表彰对健康和医学做出突出贡献的专家和学者设⽴的优秀研究奖,我的共聚焦显微镜图⽚还作为当年NHMRC年报的封⾯照⽚。
问:请与我们分享这张获奖作品背后的故事。
答:这张照⽚的拍摄相当不易,多能⼲细胞是⾮常难培养的⼀类细胞,多亏有了细胞培养、染⾊和成像⽅⾯的现代化先进技术,使我们能成功培养这些细胞,并且更加详细地观察和记录这些细胞中发⽣的⼀系列变化。每⼀次的换液、在盖玻⽚上的平铺以及⽤PBS洗涤、⽤ PFA固定等等的步骤都需要特别的耐⼼和细⼼。在细胞培养过程中,为了使细胞能更好的贴壁⽣长,我曾⽐较了多种培养基质,在多次失败、改进培养条件、再失败、再改进的过程中,最终找到了最合适细胞⽣长和实验的条件。另外,在整个实验过程中,需要我不断的摸索合适的反应条件,包括⼀抗和⼆抗的选择和稀释⽐例,⽤荧光封固剂封固,⼲燥,影像捕获等。共聚焦显微镜结合数据化图像处理技术和电⽣理等技术,可以观察细胞的⽣理活动和细胞形态及运动变化的相互关系。这些优点使它成为形态学、分⼦细胞⽣物学、神经科学和 药理学研究不可或缺的重要研究技术。
我希望这些神经⼲细胞“精彩瞬间”的美丽图⽚会让更多的⼈了解科学之美,也希望更多的⼈关注神经退⾏性疾病和医学科学的发展。
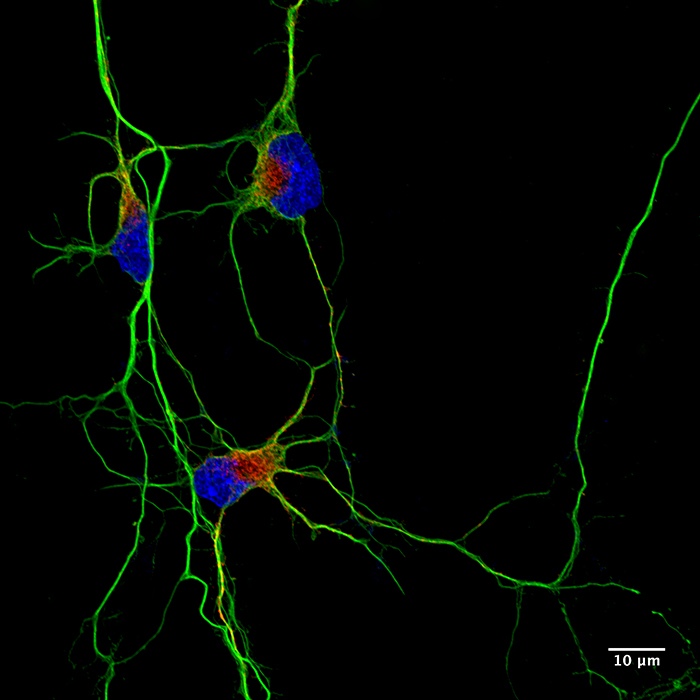
问:什么是神经⼲细胞?通过研究NSCs,您的研究的主要⽬标是什么?
答:神经⼲细胞是神经系统内的⼲细胞,可⾃我更新并演变为分化的前体细胞,从⽽⽣成各种类型的细胞如神经元及胶质细胞。我正在研究外源性α-突触核蛋⽩原纤维诱导⼈神经元细胞中病理性α-突触核蛋⽩异常积聚的形成,导致⾃噬受损和可影响其他神经元的α-突触核蛋⽩种类的释放增加,以及神经元toll样受体2 (TLR2) 有助于致病性α-突触核蛋⽩的传播。
我的研究兴趣源于⼀个⼀直让我⾮常感兴趣的主题,那就是⼈为什么会变⽼?我相信通过对不同神经细胞的疾病模型进⾏的研究可以让我们能够更好地理解这些基本问题。我们的主要⽬标是了解⼤脑进⾏⾃我清除和修复的机制,并设计旨在改善中枢神经系统损伤和神经退⾏性疾病患者的神经功能和⽣活质量改善的特定疗法。通过运⽤这些神经⼲细胞的疾病模型,我们能够研究某些⼩分⼦化合物作为PD候选药物的潜⼒,并在未来帮助患者。
问:您从这张图⽚中学到了什么?它如何帮助您了解⼈脑的分⼦和细胞特性?
答:神经⽹络和神经细胞⽐我们想象的要复杂很多。这张照⽚激发了我对⽆数的可能性的遐想,让我感到既困惑又兴奋。进⼀步研究这些神经元细胞的功能将有助于我们更好地了解中枢神经系统疾病的发⽣发展。作为⼀名神经科医⽣和神经病学科学家,我更关注⼤脑和中枢神经系统的神经通路。
在这张图⽚中,这些⼈类神经元是由神经⼲细胞分化⽽来的。细胞已被标记染⾊,这些标记描绘了神经元的细胞核(蓝⾊)和神经元之间的⽹络连接(绿⾊)、异常的蛋⽩质聚集体 (黄⾊)和⾃噬机制(红⾊)。我将免疫细胞化学技术运⽤于研究中,先⽤激活剂处理这些神经元以诱导异常蛋⽩质聚集体的形成(这是为了产⽣帕⾦森病的细胞模型),再⽤抑制剂抑制这些聚集体的积累(以便观察它是否可能成为潜在的候选药物)。我们希望通过运⽤ 些神经元进⾏的实验揭⽰神经退⾏性疾病(如帕⾦森病)的发病机制并开发新的治疗策略。
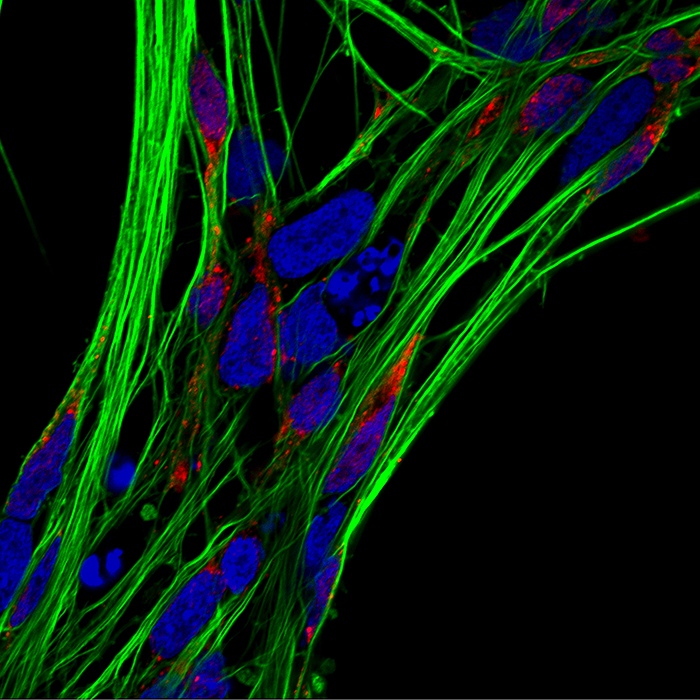
问:您使⽤什么设备和技术来拍摄如此清晰的NSC图像?
答:我⽤尼康C2共聚焦显微镜捕获得到了清晰的共聚焦显微镜照⽚。在拍摄这张照⽚时,我⽤⼀种红⾊的荧光染料标记了神经⼲细胞,⼀种绿⾊的荧光染料标记了异常的α-突触核蛋⽩聚集体,并拍摄了⼀堆⾼分辨率照⽚,这⼀切都归功于共聚焦显微镜的强⼤功能!这些成像技术不仅仅是技术,更是作为深⼊探索未知事物的强⼤⼯具。
样本的准备,显⾊剂的选择,激光和显⾊剂照射衰减等的合理配合以及空间和时间分辨率上的平衡才会成就⼀幅科学和艺术结合的图⽚。传统荧光显微镜成像质量不⾼,这使得⼀些细微结构不易被清晰地观察到。⽽共聚焦解决了焦点模糊的问题,使这些结构变得清晰可辨。 这张照⽚让我联想到了平⽇⾥吃的三明治,上下两⽚“⾯包”,中间的拉丝如同加热后的“芝⼠”,这是我拍摄完这张照⽚后的第⼀感受。除此以外,这张照⽚也让我惊奇与兴奋,因 它直观地展⽰了经过药物治疗后的帕⾦森细胞内的改变,将微观技术作为⼀种强有⼒的⼯具更好地运⽤于对微观世界的探索。
问:通过识别神经退⾏性疾病患者⼤脑中的⽣化特征,可以从中得出什么样的应⽤或治疗计划?
答:通过展⽰⼈神经元细胞中α-突触核蛋⽩的积聚和降解之间的动态关系,以及TLR2信号通路参与⼈神经元中α-突触核蛋⽩的积聚和促炎反应,为特定机制下寻找治疗帕⾦森病 (PD)的⽅法提供了证据。PD是⼀种进⾏性神经退⾏性疾病,影响了全球约700万⼈。它的病理特征是⼤脑⿊质致密部区域的多巴胺能神经元丢失,并伴有路易⼩体的形成,⽽α-突触核蛋⽩是PD病理形成中最关键的成分。我的⼯作还提供了原理证明,针对这些机制在减轻⾄少⼀部分(或更多)病理⽅⾯有⼀定的希望。因此,我的研究中建⽴起来的研究模型或可进⼀步⽤于PD的研究。并且已得到的数据⽀持使⽤⾃噬增强剂和TLR2拮抗剂来改善α-突触核蛋⽩的异常积聚,但仍需要进⼀步的⼯作来验证。我们的研究为未来研究α-突触核蛋⽩和TLR2介导的PD病理学研究提供了坚实的基础,也为利⽤这些⼩分⼦化合物找到新的治疗PD 的⽅法提供了坚实的基础。

问:除了在实验室做研究,你还喜欢什么其他的爱好或活动?
答:我是⼀名摄影爱好者,喜欢去世界各地欣赏美景,⽤我的镜头将我的主观体验和感受记录下来。我是⼀个对⾊彩特别敏感的⼈,可以⽤⾁眼观察到细微的⾊彩差别,可能这也是我痴迷于摄影的原因之⼀。我的照⽚曾被选中⽤于新西兰旅游局官⽅⽹站上的宣传照。
问:您还有什么想告诉我们的读者的吗?
答:探索神经退⾏性疾病的发病机制和治疗⽅法仍任重道远。我们感谢患者和医务⼯作者、研究⼈员、社会⼯作者等对参与这⼀旅程的热情和意愿。先进的技术在这条道路上为我们提供了便利与帮助,使过去难以实现的可视化,尤其是微观世界的可视化成为可能,并帮助我们更多地了解这⼀领域。
如果您也对神经科学感兴趣,请⼀定要坚持不懈,不断探索,因为我们所得到的点滴知识将为艰涩深奥的脑科学海洋注⼊新的⽣机与活⼒。
*****
高博士的获奖作品证明了显微技术的重要性,它帮助许多人了解自然。我们感谢高博士花时间分享他的获奖作品和他所参与的研究。我们期待他带来更多令人振奋的消息,解开人类神经退化的谜团。
高博士的联系方式:
LinkedIn: Jianqun Gao
Facebook: Jianqun Gao
Twitter: @drgaojqun
