「由外而內」策略
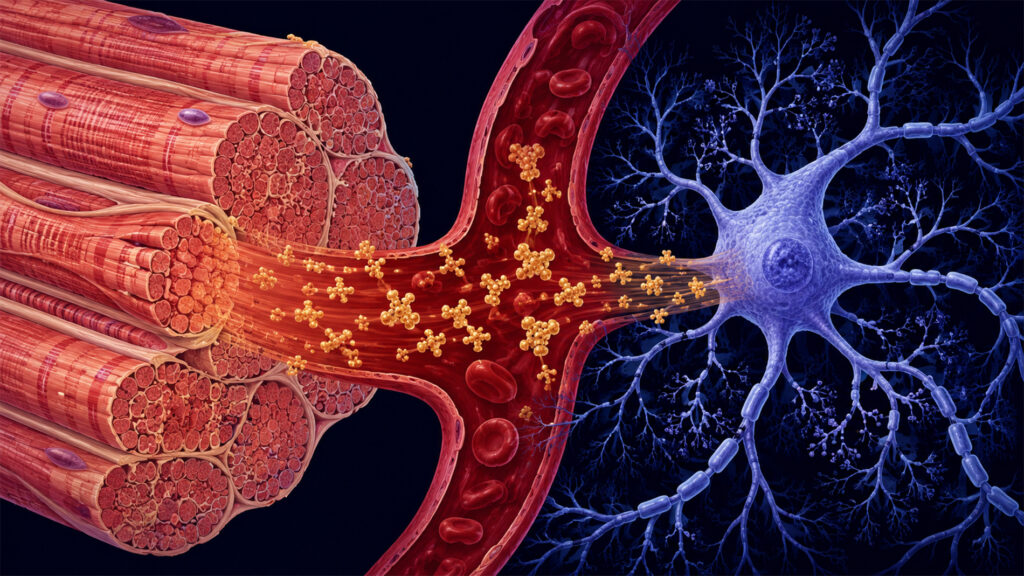
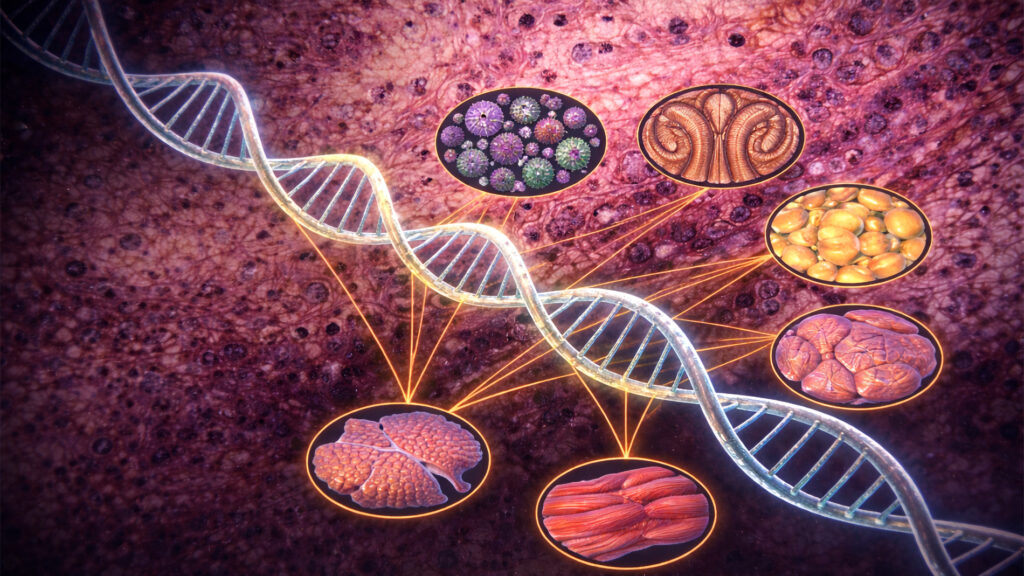
Self portrait of Henriette van Praag, Associate Professor at Florida Atlantic University’s Stiles-Nicholson Brain Institute and Charles E. Schmidt College of Medicine. Image credit: Henriette van Praag 运动肌肉释放的蛋白质,如何成为保护老化大脑的关键,且无需触碰淀粉样蛋白斑块 编者按 近一个世纪以来,医学界一直将人体视为一组专业且有些孤立的部门。心脏负责循环,肌肉负责运动,大脑则负责思考。在这种分割的模式下,像阿兹海默症这样的神经退行性疾病被视为一种局部的功能失调,也就是头骨内部的风暴,与一个人腿部的力量或握力的活力无关。 新的研究表明,骨骼肌不仅仅是机械组织,还是一种精密的内分泌器官,通过一种称为「肌动蛋白」(myokines)的分子信使流与大脑进行交流。当我们运动时,肌肉会分泌蛋白质,这些蛋白质随血液流动并穿过血脑屏障,充当神经元的维护人员。 Henriette van Praag 在佛罗里达大西洋大学 Stiles-Nicholson 大脑研究所的实验室,从一个不寻常的方向着手解决问题:从健身房而非神经病学诊所出发。二十多年前,van Praag 发现运动增加了成年啮齿动物海马体(对学习和记忆至关重要的大脑区域)中的神经发生,即新神经元的产生。这一发现启动了一场长达数十年的探索,研究体力活动如何在分子水平上与大脑进行交流。事实证明,答案可能并非始于头骨,而是始于骨骼肌。 她的实验室最近的一项研究发表在 2025 年 10 月的《老化细胞》(Aging Cell)杂志上。研究确定了 Cathepsin B(一种长期与癌症和脑损伤相关的蛋白质)作为一种肌肉来源的信号,能够在阿兹海默症小鼠模型中保留记忆和神经发生,即便淀粉样蛋白斑块和炎症依然完全存在。这是一个从「搜索与销毁」任务到「系统性修复」任务的转变。 接下来是一场关于分子信使、斑块假说的局限性、将身体视为一个系统而不止是一组器官,以及从「由外而内」治疗阿兹海默症意味着什么的对话。 — Adelina Study design: four groups of […]